მოლეკულურ-კინეტიკური თეორია საშუალებას იძლევა, სისტემის მიკროსკოპული ქცევის ანალიზით და სტატისტიკური მექანიკის მეთოდების გამოყენებით, მივიღოთ თერმოდინამიკური სისტემის მნიშვნელოვანი მაკროსკოპული მახასიათებლები. ერთ-ერთი მიკროსკოპული მახასიათებელი, რომელიც დაკავშირებულია სისტემის ტემპერატურასთან, არის გაზის მოლეკულების საშუალო კვადრატული სიჩქარე. ჩვენ ვაძლევთ მის ფორმულას და განვიხილავთ მას სტატიაში.
იდეალური გაზი
ჩვენ დაუყოვნებლივ აღვნიშნავთ, რომ გაზის მოლეკულების კვადრატული საშუალო სიჩქარის ფორმულა მოცემულია სპეციალურად იდეალური გაზისთვის. მის ქვეშ, ფიზიკაში განიხილება ისეთი მრავალნაწილაკიანი სისტემა, რომელშიც ნაწილაკები (ატომები, მოლეკულები) არ ურთიერთობენ ერთმანეთთან (მათი კინეტიკური ენერგია აღემატება ურთიერთქმედების პოტენციურ ენერგიას სიდიდის რამდენიმე რიგით) და არ აქვთ ზომები. ეს არის წერტილები სასრული მასით (ნაწილაკებს შორის მანძილი მათ ზომაზე რამდენიმე რიგით დიდი სიდიდის.წრფივი).
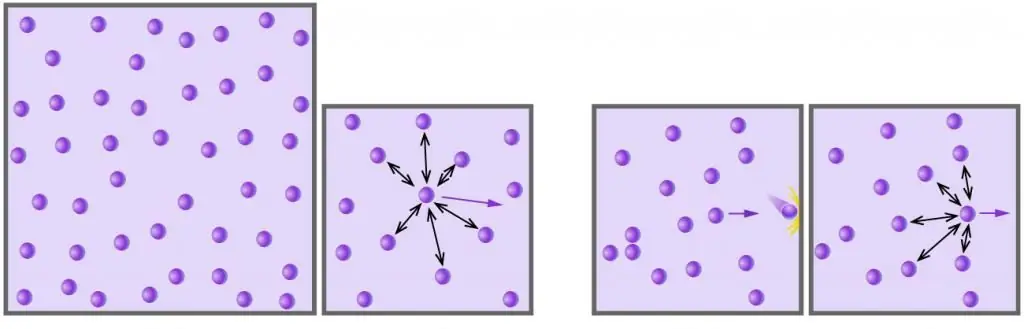
ნებისმიერი გაზი, რომელიც შედგება ქიმიურად ნეიტრალური მოლეკულებისგან ან ატომებისგან, დაბალი წნევის ქვეშ და აქვს მაღალი ტემპერატურა, შეიძლება ჩაითვალოს იდეალურად. მაგალითად, ჰაერი იდეალური აირია, მაგრამ წყლის ორთქლი აღარ არის ასეთი (წყლის მოლეკულებს შორის მოქმედებს ძლიერი წყალბადის ბმები).
მოლეკულური კინეტიკური თეორია (MKT)

MKT-ის ფარგლებში იდეალური გაზის შესწავლისას ყურადღება უნდა მიაქციოთ ორ მნიშვნელოვან პროცესს:
- გაზი ქმნის წნევას მასში შემავალი ჭურჭლის კედლებზე გადატანით, იმპულსი, როდესაც მოლეკულები და ატომები მათ ეჯახებიან. ასეთი შეჯახებები სავსებით ელასტიურია.
- გაზის მოლეკულები და ატომები მოძრაობენ შემთხვევით ყველა მიმართულებით სხვადასხვა სიჩქარით, რომელთა განაწილება ემორჩილება მაქსველ-ბოლცმანის სტატისტიკას. ნაწილაკებს შორის შეჯახების ალბათობა უკიდურესად დაბალია მათი უმნიშვნელო ზომისა და მათ შორის დიდი მანძილის გამო.
მიუხედავად იმისა, რომ გაზის ნაწილაკების ინდივიდუალური სიჩქარე ძალიან განსხვავდება ერთმანეთისგან, ამ მნიშვნელობის საშუალო მნიშვნელობა დროთა განმავლობაში უცვლელი რჩება, თუ სისტემაზე არ არის გარეგანი ზემოქმედება. გაზის მოლეკულების საშუალო კვადრატული სიჩქარის ფორმულა შეიძლება მივიღოთ კინეტიკური ენერგიისა და ტემპერატურის ურთიერთკავშირის გათვალისწინებით. ამ საკითხს სტატიის მომდევნო აბზაცში შევეხებით.
იდეალური აირის მოლეკულების კვადრატული საშუალო სიჩქარის ფორმულის წარმოშობა
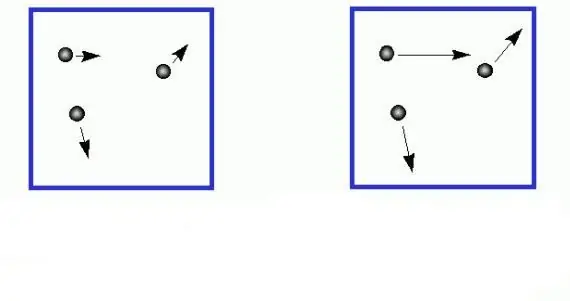
ყველა სტუდენტმა იცის ფიზიკის ზოგადი კურსიდან, რომ m მასის მქონე სხეულის გადამყვანი მოძრაობის კინეტიკური ენერგია გამოითვლება შემდეგნაირად:
Ek=mv2/2
სადაც v არის წრფივი სიჩქარე. მეორე მხრივ, ნაწილაკების კინეტიკური ენერგია ასევე შეიძლება განისაზღვროს T აბსოლუტური ტემპერატურის მიხედვით, გარდაქმნის ფაქტორის გამოყენებით kB (ბოლცმანის მუდმივი). ვინაიდან ჩვენი სივრცე სამგანზომილებიანია, Ek გამოითვლება შემდეგნაირად:
Ek=3/2kBT.
ეკვივალენტური ორივე ტოლობის და გამოვსახავთ v მათგან, ვიღებთ ფორმულას კვადრატული იდეალური აირის საშუალო სიჩქარისთვის:
mv2/2=3/2kBT=>
v=√(3kBT/მ).
ამ ფორმულაში m - არის გაზის ნაწილაკების მასა. მისი მნიშვნელობა არასასიამოვნოა პრაქტიკულ გამოთვლებში გამოსაყენებლად, რადგან ის მცირეა (≈ 10-27 კგ). ამ უხერხულობის თავიდან ასაცილებლად, გავიხსენოთ უნივერსალური აირის მუდმივა R და მოლური მასა M. მუდმივა R kB-ით დაკავშირებულია ტოლობით:
kB=R/NA.
M-ის მნიშვნელობა განისაზღვრება შემდეგნაირად:
M=mNA.
ორივე ტოლობის გათვალისწინებით, ჩვენ ვიღებთ შემდეგ გამოსახულებას მოლეკულების ფესვის საშუალო კვადრატული სიჩქარისთვის:
v=√(3RT/M).
ამგვარად, გაზის ნაწილაკების საშუალო კვადრატული სიჩქარე პირდაპირპროპორციულია აბსოლუტური ტემპერატურის კვადრატული ფესვისა და უკუპროპორციულია მოლური მასის კვადრატული ფესვისა.
პრობლემის გადაჭრის მაგალითი
ყველამ იცის, რომ ჰაერი, რომელსაც ჩვენ ვსუნთქავთ, არის 99% აზოტი და ჟანგბადი. საჭიროა N2 და O2 მოლეკულების საშუალო სიჩქარეებში განსხვავებების დადგენა 15 o ტემპერატურაზე. C.

ეს პრობლემა თანმიმდევრულად მოგვარდება. პირველ რიგში, ჩვენ ვთარგმნით ტემპერატურას აბსოლუტურ ერთეულებში, გვაქვს:
T=273, 15 + 15=288, 15 K.
ახლა დაწერეთ მოლური მასები თითოეული განხილული მოლეკულისთვის:
MN2=0.028 კგ/მოლი;
MO2=0.032 კგ/მოლი.
რადგან მოლური მასების მნიშვნელობები ოდნავ განსხვავდება, მათი საშუალო სიჩქარეც იმავე ტემპერატურაზე ახლოს უნდა იყოს. v ფორმულის გამოყენებით, ჩვენ ვიღებთ შემდეგ მნიშვნელობებს აზოტისა და ჟანგბადის მოლეკულებისთვის:
v (N2)=√(38, 314288, 15/0, 028)=506,6 მ/წმ;
v (O2)=√(38, 314288, 15/0, 032)=473,9 მ/წმ.
რადგან აზოტის მოლეკულები ოდნავ მსუბუქია ჟანგბადის მოლეკულებზე, ისინი უფრო სწრაფად მოძრაობენ. საშუალო სიჩქარის სხვაობაა:
v (N2) - v (O2)=506,6 - 473,9=32,7 მ/წმ.
მიღებული მნიშვნელობა არის აზოტის მოლეკულების საშუალო სიჩქარის მხოლოდ 6,5%. ჩვენ ყურადღებას ვაქცევთ აირებში მოლეკულების მაღალ სიჩქარეს, თუნდაც დაბალ ტემპერატურაზე.






