თერმოდინამიკაში სისტემის საწყისიდან საბოლოო მდგომარეობიდან გადასვლის შესწავლისას მნიშვნელოვანია იცოდეთ პროცესის თერმული ეფექტი. სითბოს სიმძლავრის კონცეფცია მჭიდროდ არის დაკავშირებული ამ ეფექტთან. ამ სტატიაში განვიხილავთ კითხვას, თუ რა იგულისხმება აირის იზოქორული სითბოს სიმძლავრეში.
იდეალური გაზი
იდეალური აირი არის გაზი, რომლის ნაწილაკები ითვლება მატერიალურ წერტილებად, ანუ მათ არ აქვთ ზომები, მაგრამ აქვთ მასა და რომელშიც მთელი შინაგანი ენერგია შედგება მხოლოდ მოლეკულების მოძრაობის კინეტიკური ენერგიისგან. და ატომები.
ნებისმიერი რეალური აირი იდეალურად არასოდეს დააკმაყოფილებს აღწერილ მოდელს, რადგან მის ნაწილაკებს ჯერ კიდევ აქვთ გარკვეული ხაზოვანი ზომები და ურთიერთქმედებენ ერთმანეთთან სუსტი ვან დერ ვაალსის ბმების ან სხვა ტიპის ქიმიური ბმების გამოყენებით. თუმცა, დაბალ წნევაზე და მაღალ ტემპერატურაზე მოლეკულებს შორის მანძილი დიდია და მათი კინეტიკური ენერგია ათჯერ აჭარბებს პოტენციურ ენერგიას. ეს ყველაფერი შესაძლებელს ხდის რეალური გაზებისთვის იდეალური მოდელის მაღალი სიზუსტით გამოყენებას.
გაზის შიდა ენერგია
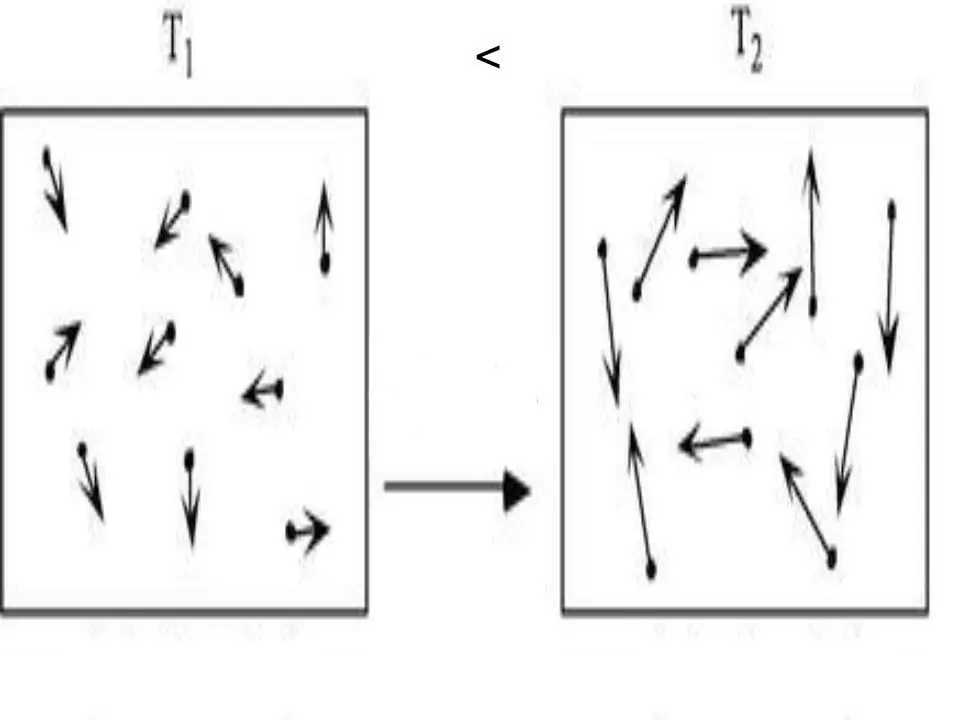
ნებისმიერი სისტემის შინაგანი ენერგია არის ფიზიკური მახასიათებელი, რომელიც უდრის პოტენციური და კინეტიკური ენერგიის ჯამს. ვინაიდან იდეალურ აირებში პოტენციური ენერგიის უგულებელყოფა შეიძლება, ჩვენ შეგვიძლია დავწეროთ მათ ტოლობა:
U=Ek.
სადაც Ek არის კინეტიკური სისტემის ენერგია. მოლეკულური კინეტიკური თეორიის გამოყენებით და უნივერსალური კლაპეირონ-მენდელეევის განტოლების გამოყენებით U-ს გამოთქმის მიღება არ არის რთული. ქვემოთ წერია:
U=z/2nRT.
აქ T, R და n არის აბსოლუტური ტემპერატურა, აირის მუდმივი და ნივთიერების რაოდენობა, შესაბამისად. z-მნიშვნელობა არის მთელი რიცხვი, რომელიც მიუთითებს გაზის მოლეკულის თავისუფლების ხარისხების რაოდენობაზე.
იზობარული და იზოქორული სითბოს სიმძლავრე
ფიზიკაში სითბური სიმძლავრე არის სითბოს რაოდენობა, რომელიც უნდა მიეწოდოს შესასწავლ სისტემას, რათა გაათბოს იგი ერთი კელვინით. საპირისპირო განმარტებაც მართალია, ანუ თბოტევადობა არის სითბოს რაოდენობა, რომელსაც სისტემა გამოყოფს ერთი კელვინით გაცივებისას.
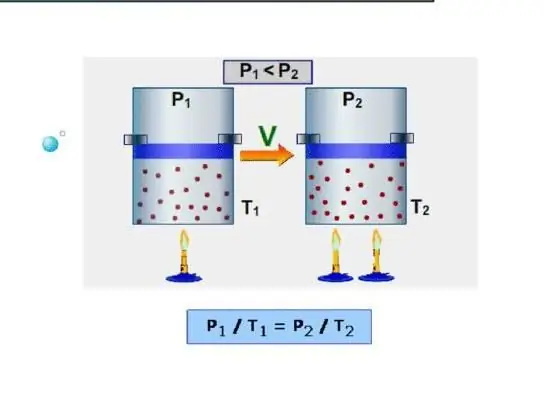
სისტემისთვის ყველაზე მარტივი გზაა იზოქორული სითბოს სიმძლავრის განსაზღვრა. ეს გაგებულია, როგორც სითბოს სიმძლავრე მუდმივი მოცულობით. ვინაიდან სისტემა არ ასრულებს სამუშაოს ასეთ პირობებში, მთელი ენერგია იხარჯება ენერგიის შიდა რეზერვების გაზრდაზე. მოდით ავღნიშნოთ იზოქორული სითბოს სიმძლავრე სიმბოლო CV, შემდეგ შეგვიძლია დავწეროთ:
dU=CVdT.
ანუ შინაგანი ენერგიის ცვლილებასისტემა პირდაპირპროპორციულია მისი ტემპერატურის ცვლილებისა. თუ ამ გამოთქმას შევადარებთ წინა აბზაცში დაწერილ ტოლობას, მაშინ მივიღებთ ფორმულას CV იდეალურ აირში:
СV=z/2nR.
ეს მნიშვნელობა არასასიამოვნოა პრაქტიკაში გამოსაყენებლად, რადგან ეს დამოკიდებულია სისტემაში არსებული ნივთიერების რაოდენობაზე. ამრიგად, დაინერგა სპეციფიკური იზოქორული სითბოს სიმძლავრის კონცეფცია, ანუ მნიშვნელობა, რომელიც გამოითვლება ან 1 მოლ გაზზე ან 1 კგ-ზე. პირველი მნიშვნელობა ავღნიშნოთ სიმბოლოთი CV, მეორე - სიმბოლო CV. მ. მათთვის შეგიძლიათ დაწეროთ შემდეგი ფორმულები:
CV=z/2R;
CVმ=z/2R/M.
აქ M არის მოლური მასა.
იზობარი არის სითბოს სიმძლავრე სისტემაში მუდმივი წნევის შენარჩუნებისას. ასეთი პროცესის მაგალითია გაზის გაფართოება ცილინდრში დგუშის ქვეშ მისი გაცხელებისას. იზოქორული პროცესისგან განსხვავებით, იზობარული პროცესის დროს სისტემაში მიწოდებული სითბო იხარჯება შიდა ენერგიის გასაზრდელად და მექანიკური სამუშაოების შესასრულებლად, ანუ:
H=dU + PdV.
იზობარული პროცესის ენთალპია არის იზობარული სითბური სიმძლავრის და სისტემაში ტემპერატურის ცვლილების პროდუქტი, ანუ:
H=CPdT.
თუ განვიხილავთ გაფართოებას 1 მოლი აირის მუდმივ წნევაზე, მაშინ თერმოდინამიკის პირველი კანონი დაიწერება როგორც:
CPdT=CV dT + RdT.
ბოლო წევრი მიიღება განტოლებიდანკლაპეირონ-მენდელეევი. ამ თანასწორობიდან გამომდინარეობს კავშირი იზობარულ და იზოქორიულ სითბოს სიმძლავრეებს შორის:
CP=CV + R.
იდეალური გაზისთვის, მუდმივი წნევის დროს სპეციფიკური მოლური სითბოს სიმძლავრე ყოველთვის მეტია შესაბამის იზოქორიულ მახასიათებელზე R=8, 314 J/(molK).
მოლეკულების თავისუფლების ხარისხი და სითბოს მოცულობა
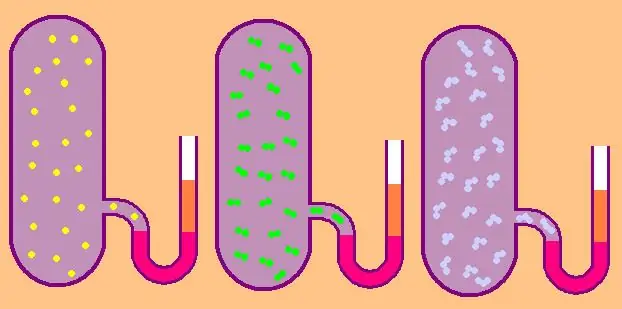
მოდით ისევ დავწეროთ ფორმულა კონკრეტული მოლური იზოქორული სითბოს სიმძლავრისთვის:
CV=z/2R.
მონატომური აირის შემთხვევაში, მნიშვნელობა z=3, რადგან სივრცეში ატომებს შეუძლიათ გადაადგილება მხოლოდ სამი დამოუკიდებელი მიმართულებით.
თუ ვსაუბრობთ გაზზე, რომელიც შედგება დიატომური მოლეკულებისგან, მაგალითად, ჟანგბადი O2 ან წყალბადი H2, მაშინ, გარდა მთარგმნელობითი მოძრაობისა, ამ მოლეკულებს მაინც შეუძლიათ ბრუნავენ ორი ერთმანეთის პერპენდიკულარული ღერძის გარშემო, ანუ z უდრის 5.
უფრო რთული მოლეკულებისთვის გამოიყენეთ z=6. CV






